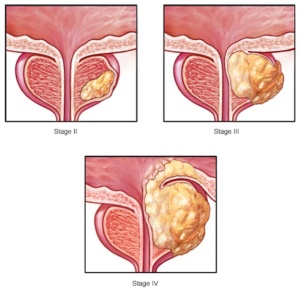
АДЕНОМА ПРОСТАТЫ (ДОБРОКАЧЕСТВЕННАЯ ГИПЕРПЛАЗИЯ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ)
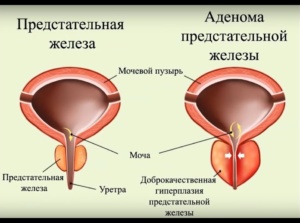 Фермент 5-альфа-редуктаза играет важную роль в регуляции роста волос и развитии доброкачественной гиперплазии предстательной железы (ДГПЖ). К настоящему времени обнаружено 2 типа этого фермента – I и II. 5-альфа-редуктаза I типа обладает незначительной активностью в тканях простаты и представлена в основном в коже и печени, 5-альфа-редуктаза II типа локализуется чаще всего в предстательной железе и преобразует мужской половой гормон тестостерон в более активную форму дигидротестостерон, который более активно связывается с андрогенными рецепторами тканей, чем тестостерон. Считается, что повышенное образование дигидротестостерона из тестостерона в тканях простаты приводит к развитию ДГПЖ.
Фермент 5-альфа-редуктаза играет важную роль в регуляции роста волос и развитии доброкачественной гиперплазии предстательной железы (ДГПЖ). К настоящему времени обнаружено 2 типа этого фермента – I и II. 5-альфа-редуктаза I типа обладает незначительной активностью в тканях простаты и представлена в основном в коже и печени, 5-альфа-редуктаза II типа локализуется чаще всего в предстательной железе и преобразует мужской половой гормон тестостерон в более активную форму дигидротестостерон, который более активно связывается с андрогенными рецепторами тканей, чем тестостерон. Считается, что повышенное образование дигидротестостерона из тестостерона в тканях простаты приводит к развитию ДГПЖ.
Для лечения этого недуга обычно назначают ингибиторы 5-альфа-редуктазы. Блокируя 5-альфа-редуктазу, они снижают концентрацию дигидротестостерона, индуцируют апоптоз простатических эпителиальных клеток, при длительном применении уменьшают объем простаты в среднем на 15-25% и увеличивают пиковую скорость мочеиспускания, устраняя, таким образом механический компонент обструкции при ДГПЖ. [Gravas & Oelke, 2010].
Сегодня основными препаратами лечения ДГПЖ являются синтетические стероидные препараты – финастерид и дутастерид, но они обладают серьезными побочными эффектами. В частности, в Великобритании за год было зарегистрировано 50 случаев развития рака молочной железы у мужчин, принимавших препарат финастерид в дозе 5 мг, и 3 случая – при использовании препарата в дозе 1 мг [Финастерид: рак …, 2011]. Поэтому контрольно-разрешительный орган США (FDA) предостерегает о том, что прием этих средств повышает риск развития тяжелых форм рака предстательной железы и молочных желез [Финастерид и Дутастерид…, 2011].
В связи с этим, активно ведутся поиски и разработка безопасных, главным образом растительных, средств – ингибиторов фермента 5-альфа-редуктаза II типа. В настоящее время выявлен ряд растений, обладающих подобным действием. Из них на данный момент лучше всего изучены корневища крапивы двудомной (Urtica dioica), плоды пальмы сабаль (Serenoa repens), кора африканской сливы (Pygeum africanum).
Наряду с вышеуказанными растениями сильное тормозящее действие на активность 5-альфа-редуктазы II типа показал экстракт софоры желтеющей.
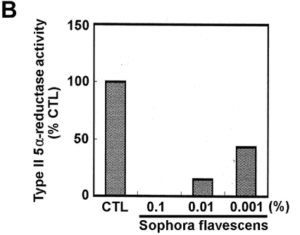
Так, исследователями из Южной Кореи в эсперименте было установлено, что в клетках предстательной железы крыс 0,1% экстракт софоры желтеющей полностью подавляет активность фермента 5-альфа-редуктаза II типа, а 0,001% раствор ингибирует его на 50% (Рис.3) [Roh et al., 2002]. Эти данные позволяют сделать вывод, что софора желтеющая является перспективным растением для создания препаратов способных эффективно подавлять развитие ДГПЖ.
Воздействие экстрактов софоры желтеющей на активность 5-альфа-редуктазы 2-го типа изучено на простате крыс. После инкубации ткани стероиды были экстрагированы, разделены на ТСХ пластине, а затем проявлены методом авторадиографии с помощью пленки «Hyperfilm», плотность окраски пятен определена на денситометре.
Рис.(А) Репрезентативная авторадиограмма результатов исследования активности 5-альфа-редуктазы 2-го типа.
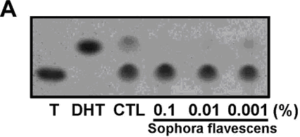
Рис.(А) Репрезентативная авторадиограмма результатов исследования активности 5-альфа-редуктазы 2-го типа.
Рис.(B) Количественная оценка активности 5-α-редуктазы 2-го типа.
- T — тестостерон;
- DHT — дигидротестостерон;
- CTL — контроль;
- 0.1 — софоры желтеющей экстракт 0,1%;
- 0.01 — софоры желтеющей экстракт 0,01%;
- 0.001 — софоры желтеющей экстракт 0,001%.
Представлены коэффициенты конвертации Т в ДГТ, которые выражены в процентах от контроля.
Литература
- Финастерид: рак молочной железы у мужчин // Безопасность лекарств и фармаконадзор. 2011. №3. С. 35-36.
- Финастерид и Дутастерид: повышенный риск развития рака простаты // Безопасность лекарств и фармаконадзор. 2011. №3. С. 24.
- Gravas S., Oelke M. Current status of 5a-reductase inhibitors in the management of lower urinary tract symptoms and BPH // World J. Urol. 2010. Vol. 28. P. 9-15.
- Roh SS, Kim CD, Lee MH, Hwang SL, Rang MJ Yoon YK. The hair growth promoting effect of Sophora flavescens extract and its molecular regulation// J Dermatological Sci. 2002. 30: 43-49.
РАК ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
Установлено, что основные алкалоиды софоры желтеющей матрин и оксиматрин, а также некоторые ее флавоноиды в эксперименте обладают способностью оказывать ингибирующее действие на раковые клетки предстательной железы [Chen et al., 2008a, b; Wu et al., 2015; Zhang et al., 2012].
Рак предстательной железы (РПЖ) является одной из наиболее распространенных форм рака у мужчин в странах Запада, а в ряде стран стоит на втором месте в списке ведущих причин смерти от рака у мужчин. В Европе ежегодно регистрируется около 300 000 новых случаев рака предстательной железы. В мировом масштабе этот показатель достигает 670 000.
Рак предстательной железы в России занимает 4 место после рака легкого, желудка и немеланомных образований кожи. По величине прироста (в 2,8 раза) показателя заболеваемости в России за период с 1999 г. по 2009 г. РПЖ занял 1-е место. На долю опухолей предстательной железы приходится 6,9% от всех злокачественных новообразований у мужчин. Смертность от РПЖ составляет 10,4 на 100 тыс. мужского населения [Казанцев, Стрыгина, 2014].
Матрин в эксперименте in vitro оказывает ингибирующее действие как на андрогеннечувствительные клетки рака простаты (PC-3) [Zhang et al., 2012], так и на андрогенчувствительные клетки простаты линии (LNCap). [Chen K, et al., 2008а]. В последнем исследовании, матрин в концентрациях 0,5; 1,0; 1,5 и 2,0 г/л в течение 12, 24 и 36 часов показал дозо- и времязависимое ингибирование пролиферации раковых клеток до 56,8% при максимальных дозе и времени (2 г/л в течение 36 часов). Кроме того, было отмечено значительное снижение численности андрогенных рецепторов (более чем на 50%) при самой низкой дозе (0,5 г/л) после 24 часов. В другом исследовании эти же авторы подтвердили, что матрин может значительно подавлять рост LNCaP клеток, ингибировать экспрессию простатического специфического антигена (ПСА) и андрогенных рецепторов раковых клеток простаты. По их мнению, матрин может быть использован в терапии рака простаты, но в настоящее время пока нет исследований на животных. [Chen K, et al., 2008b].
 В результате исследования действия оксиматрина на раковые клетки простаты было установлено, что он обладает теми же свойствами, что и матрин. В частности, МТТ-тест* показал, что оксиматрин значительно ингибирует пролиферацию клеток рака простаты время- и дозозависимым образом. Кроме того, при помощи TUNEL-метода и проточной цитометрии установлено, что воздействие оксиматрина может индуцировать апоптоз клеток рака простаты в зависимости от дозы. Более того, вестерн-блот анализ показал значительное увеличение экспрессии маркеров апоптоза p53 и bax и значительное снижение Bcl-2, в клетках рака простаты в зависимости от дозы. Исследования in vivo показали, что оксиматрин ингибирует рост опухоли после подкожной прививки клеток рака простаты у голых мышей. Результаты этой работы свидетельствуют, что противоопухолевые свойства оксиматрина связаны с ингибированием пролиферации клеток и индукции апоптоза путем регуляции апоптоз-ассоциированной экспрессии генов, что может обеспечить новый подход к разработке терапии рака простаты с использованием оксиматрина [Wu et al., 2015].
В результате исследования действия оксиматрина на раковые клетки простаты было установлено, что он обладает теми же свойствами, что и матрин. В частности, МТТ-тест* показал, что оксиматрин значительно ингибирует пролиферацию клеток рака простаты время- и дозозависимым образом. Кроме того, при помощи TUNEL-метода и проточной цитометрии установлено, что воздействие оксиматрина может индуцировать апоптоз клеток рака простаты в зависимости от дозы. Более того, вестерн-блот анализ показал значительное увеличение экспрессии маркеров апоптоза p53 и bax и значительное снижение Bcl-2, в клетках рака простаты в зависимости от дозы. Исследования in vivo показали, что оксиматрин ингибирует рост опухоли после подкожной прививки клеток рака простаты у голых мышей. Результаты этой работы свидетельствуют, что противоопухолевые свойства оксиматрина связаны с ингибированием пролиферации клеток и индукции апоптоза путем регуляции апоптоз-ассоциированной экспрессии генов, что может обеспечить новый подход к разработке терапии рака простаты с использованием оксиматрина [Wu et al., 2015].
Среди флавоноидов софоры желтеющей наиболее сильное ингибирующее действие на андрогенные рецепторы показали, норкураринон и изокураринон при концентрации 50-200 мг/мл с уровнем ингибирования 51,4-94,2% и 54,4-97,1% соответственно, хотя многие другие флавоноидные соединения, также проявляли ингибирующие свойства особенно в концентрации 200 мг/мл. [Kuroyanagi et al., 1999].
*MTT-тест используется для оценки цитотоксичности потенциально противоопухолевых соединений.
Литература
- Казанцева М. В., Стрыгина Е. А. Эффективность Фирмагона при распространённом раке предстательной железы после прогрессирования на стандартной схеме МАБ: разбор клинического случая // Злокачественные опухоли. 2014. № 1 (8). С. 47-51.
- Chen K, Hu ZQ, Wang T, Guo JL, Guo H, Ye ZQ. Matrine inhibits the proliferation of prostate cancer cells and the activity of androgen receptor // Zhonghua Nan Ke Xue. 2008 а. Aug; 14(8):719-22.
- Chen K, Hu Z, Wang T, Guo H, Ye Z. Inhibitory effect of matrine on the expression of PSA and AR in prostate cancer cell line LNCaP// J Huazhong Univ Sci Technolog Med Sci. 2008 b. Dec; 28(6):697-9.
- Kuroyanagi M., Arakawa Т., Hirayama Y., Hayashi T. Antibacterial and antiandrogen flavonoids from Sophora flavescens // J. Nat. Prod. 1999. Vol. 62, N 12. P. 1595-1599
- Wu C, Huang W, Guo Y, Xia P, Sun X, Pan X, Hu W. Oxymatrine inhibits the proliferation of prostate cancer cells in vitro and in vivo // Mol Med Rep. 2015. Jun; 11(6):4129-34.
- Zhang P, Wang Z, Chong T, Ji Z. Matrine inhibits proliferation and induces apoptosis of the androgenindependent prostate cancer cell line PC-3 // Mol Med Report. 2012. Mar; 5(3):783-7.
ЭРЕКТИЛЬНАЯ ДИСФУНКЦИЯ
 Причины, приводящие к нарушению эрекции разнообразны: расстройства кровообращения полового члена в результате атеросклероза, сахарного диабета, заболеваний и повреждений пещеристых тел полового члена; расстройства иннервации; гормональных расстройств; депрессии и многих других. Эти разнообразные этиологические факторы лежат в основе различных патогенетических механизмов развития эректильной дисфункции.
Причины, приводящие к нарушению эрекции разнообразны: расстройства кровообращения полового члена в результате атеросклероза, сахарного диабета, заболеваний и повреждений пещеристых тел полового члена; расстройства иннервации; гормональных расстройств; депрессии и многих других. Эти разнообразные этиологические факторы лежат в основе различных патогенетических механизмов развития эректильной дисфункции.
Среди них важная роль принадлежит ферменту фосфодиэстераза 5 типа (ФДЭ-5), которая метаболизирует циклический гуанозинмонофосфат (цГМФ), играющий главную роль в механизме эрекции. Основным эффектом цГМФ является расслабление гладкой мускулатуры, расширение сосудов и повышенное кровенаполнение полового члена.
В настоящее время для улучшения эрекции используют главным образом синтетические ингибиторы ФДЭ-5. Из них в России наиболее используемы следующие: Силденафил (Виагра, Динамико), Варденафил (Левитра), Тадалафил (Сиалис), Уденафил (Зидена).
Ингибиторы ФДЭ-5 не обладают абсолютной селективностью в отношении ФДЭ-5 и частично подавляют активность других изоформ этого фермента: ФДЭ-1, ФДЭ-6, ФДЭ-11. Это приводит к накоплению цГМФ не только в половом члене, но и в других органах. Именно с этим связано проявление различных побочных эффектов ингибиторов ФДЭ-5 [Gresser & Gleiter, 2002]. ЦГМФ участвует в самых разнообразных сигнальных путях, выполняя роль активатора протеинкиназ. Поэтому и побочные эффекты, связанные с избытком цГМФ в разных органах очень вариабельны.
В этой связи сейчас активно ведутся поиски природных селективных ингибиторов ФДЭ-5, не оказывающих влияния на другие типы ФДЭ. В частности, in vitro было установлено, что экстракты из софоры желтеющей обладают сильной ингибирующей активностью в отношении ФДЭ-5, полученной из диафрагмы крыс. Из пяти исследованных флавоноидов софоры желтеющей (кушенол H, кушенол K, кураринол, софофлавесценол и кураридин) прениловый флавонол софофофлавесценол оказался самым сильным селективным ингибитором ФДЭ-5 с *IC50 = 0,013 мкM, тогда как наиболее известный сегодня природный ингибитор ФДЭ-5 икариин, выделенный из горянки (Epimedium brevicornum), имеет значение IC50 = 5,9 мкM [Dell’Agli et al., 2008]. Для сравнения IC50 ФДЭ-5 для Виагры составляет 0,003 мкM. [Shin et al., 2002]. Избирательность cофофофлавесценола в отношении ФДЭ-5 была больше, чем в отношении ФДЭ-3 и ФДЭ-4 в 31,5 раза и 196,2 раза, соответственно [Shin et al., 2002].
Поскольку софофлавесценол не связан структурно с другими известными ингибиторами цГМФ ФДЭ-5, которые были синтезированы путем модификации структуры силденафила, то это соединение можно рассматривать в качестве перспективного вещества для синтеза селективных и эффективных ингибиторов цГМФ ФДЭ-5 со значительно меньшим количеством побочных эффектов по сравнению с Виагрой и ее производными [Shin et al., 2002].
*IC50 — концентрация полумаксимального ингибирования
Литература
- Dell’Agli M, Galli GV, Dal Cero E, Belluti F, Matera R, Zironi E, Pagliuca G, Bosisio E. Potent inhibition of human phosphodiesterase-5 by icariin derivatives // J Nat Prod. 2008 Sep; 71(9):1513-1517.
- Gresser U, Gleiter CH. Erectile dysfunction: comparison of efficacy and side effects of the PDE-5 inhibitors sildenafil, vardenafil and tadalafil review of the literature. //Eur J Med Res. 2002. Vol. 7, N 10. P. 435-446.
- Shin HJ1, Kim HJ, Kwak JH, Chun HO, Kim JH, Park H, Kim DH, Lee YS. A prenylated flavonol, sophoflavescenol: a potent and selective inhibitor of cGMP phosphodiesterase 5 // Bioorg Med Chem Lett. 2002. Sep 2; 12(17):2313-6.